hiPSC 유래 혈관 장기 온 칩: 단방향 흐름을 통한 생리학적 정렬 달성
관류의 정밀한 제어는 생리학적 관련성을 갖춘 장기 온 칩 (OoC) 모델의 근간입니다. 록킹 플랫폼과 복잡한 수동 설정은 종종 한계가 있으나, Omi™ OoC 플랫폼은 장기적인 단방향 재순환을 위한 컴팩트하고 자동화된 솔루션을 제공합니다.
라이덴 장기 온 칩 센터와 협력하여 개발된 본 애플리케이션 노트는 안정적인 흐름이 hiPSC 유래 혈관 모델에서 우수한 내피 세포 정렬 및 극화를 어떻게 유도하는지 보여줍니다.
본 연구는 라이덴 장기 온 칩 센터 및 라이덴 대학교 의료원 오를로바 연구 그룹 소속 다니시 카시 박사, 한나 라메르트세 박사, 발레리아 오를로바 박사와의 협력 하에 수행되었습니다.


과제: 단방향 흐름이 중요한 이유
체외 모델은 동물 실험을 보완하고 줄이며 잠재적으로 대체함으로써 생의학 연구에 혁신을 가져올 잠재력을 지니고 있습니다. 인간 유도 만능 줄기세포 (hiPSC) 및 장기 특이적 세포 분화 프로토콜과 결합하면, 첨단 인간 체외 모델을 설계하여 신약 개발, 인간 질병 규명, 그리고 맞춤형 의학 구현이 가능해집니다¹,². 미세유체 장기 온 칩 (OoC) 모델은 특히 이에 적합합니다. 미세 크기의 관류 챔버 내에 생체 인간 세포를 수용하여 조직 및 장기 기능을 소형화된 포맷으로 모사할 수 있기 때문입니다¹–³.
인체 내에서 건강한 동맥과 정맥은 지속적이고 층류 (laminar) 형태의 전단 응력을 경험합니다. 이를 체외에서 재현하기 위해서는 정적 조건이나 양방향 (록킹) 흐름으로는 불충분합니다.
- 정적 배양 (Static Culture): 생리학적이지 않은 “자갈돌 (cobblestone)” 형태의 세포 형태를 유도합니다.
- 양방향 흐름 (Bidirectional Flow): 교란된 병리적 조건 (예: 동맥경화증) 을 모사합니다.
- 단방향 흐름 (Unidirectional Flow): 성숙하고 안정된 내피 세포 표현형 유도에 필수적입니다.
해결책: Omi™ OoC 플랫폼
Fluigent 의 Omi 는 컴팩트하고 사용하기 쉬운 미세유체 시스템으로, 연구자가 원하는 장기 온 칩 모델을 연결하고 재순환 기능을 갖춘 단방향 미세유체 흐름 실험을 설정할 수 있게 해줍니다. Omi™ 는 복잡한 미세유체 공학을 사용자 친화적이고 자동화된 시스템으로 단순화합니다.
혈관 모델링을 위한 주요 기능:
- 지속적 재순환 (Continuous Recirculation): 최소량의 배지 (3.3 mL) 로 5 일 이상 안정적인 흐름 프로파일을 유지합니다.
- 범용 호환성 (Universal Compatibility): 표준 Luer 피팅을 통해 모든 칩 (예: Beonchip Be-Flow) 과 연결 가능합니다.
- 스마트 제어 (Smart Control): 정밀한 캘리브레이션 및 흐름 스케줄링을 위한 직관적인 Android 인터페이스를 제공합니다.
실험 결과: 한눈에 보기
본 애플리케이션 노트에서는 hiPSC 유래 내피 세포 (hiPSC-ECs)⁴,⁵ 를 접종한 Beonchip Be-Flow 칩을 Omi 시스템에 연결하여 5 일간 단방향 흐름 실험을 수행했습니다. 이 조건은 정적 조건으로 배양된 칩 및 록킹 플랫폼에서 양방향 흐름을 적용한 칩과 비교되었습니다.
| 특징 | 정적 (Static) | 양방향 (록킹) | Omi™ 단방향 |
|---|---|---|---|
| 흐름 프로파일 | 흐름 없음 | 간헐적/역방향 | 안정적/지속적 |
| 세포 형태 | 자갈돌 (Cobblestone) | 무작위 | 길쭉하고 정렬됨 |
| 극화 (Polarization) | 없음 | 낮음 (0.024) | 강함 (0.174) |
| 전단 응력 | 0 dyn/cm2 | 가변적 | 0.912 dyn/cm² |
실험 워크플로우 및 정량적 판독값: 5 일 자동화 워크플로우
본 애플리케이션 노트는 세포 접종부터 정량적 이미지 분석까지 단계별 실험 워크플로우를 제공합니다.
다음 내용을 확인할 수 있습니다:
- hiPSC 유래 내피 세포를 위한 5 일간 단방향 흐름 프로토콜
- Omi™ 설정 및 재순환 워크플로우
- 정적, 양방향 및 단방향 흐름 조건의 비교
- PolarityJam 을 활용한 세포 정렬 및 극화의 정량적 분석
- 장기 배양 기간 동안 안정적인 흐름 유지에 대한 증거
1. 세포 분화 및 배양 + 세포 접종
hiPSC 는 재조합 비트로넥틴 (vitronectin) 이 코팅된 플레이트에서 TeSR-E8 배지를 사용하여 배양하였으며, 주 1 회 계대 배양을 수행했습니다. hiPSC 유래 내피 세포 (hiPSC-ECs) 는 오를로바 연구 그룹에서 ранее 보고된 방법에 따라 분화 및 배양되었습니다⁴,⁵. Beonchip Be-Flow 미세유체 칩은 50 µg/mL 소 혈장 피브로넥틴 (bovine fibronectin) 으로 코팅하였습니다. hiPSC-ECs 를 해리시킨 후, PenStrep 이 보충된 EGM-2 배지에 5×10⁶ cells/mL 농도로 재현탁하였습니다. 50 µL 의 세포 현탁액을 칩 주입구에 조심스럽게 피펫팅하여 세포가 수동적으로 칩 내부로 주입되도록 하였습니다. 세포는 37°C 에서 1 시간 동안 부착되도록 한 후, 칩을 록킹 플랫폼으로 옮겨 15 시간 (하룻밤) 동안 배양하였습니다.
다음 날, 칩을 정적 조건으로 두거나, 록킹 플랫폼 (양방향 흐름) 에 유지하거나, Omi 에 연결 (단방향 흐름) 하여 실험을 시작하였습니다.
2. Omi 설정
자동화된 5 일 재순환 프로토콜을 Omi 소프트웨어를 사용하여 작성하고, Omi 장치에 로드하였습니다 (그림 2A). 소프트웨어는 내장된 단계별 안내를 통해 각 단계를 안내하며, 주요 절차는 다음과 같습니다:
- 캘리브레이션 (Calibration): 정확한 흐름 측정을 위해 저장소 레벨 센서를 설정합니다.
- 멸균 (Sterilization): Omi 유체 경로 및 실험용 튜브를 물로 세척한 후 70% 에탄올로 처리합니다. 참고: 사용 전 모든 커넥터 및 튜브는 오토클레이브 멸균 또는 멸균액 보관을 통해 미리 멸균 처리하였습니다.
- 로딩 (Loading): 기포 제거 및 지속적 흐름 확보를 위해 배지로 유체 경로를 미리 채웁니다.
- 칩 연결 (Chip Connection): 재순환 시작 전, Omi 를 미세유체 칩 (Beonchip Be-Flow) 에 연결합니다 (그림 2).
hiPSC-ECs 를 포함한 미세유체 칩 (Beonchip Be-Flow) 은 표준 Luer 피팅 및 미세유체 튜빙을 사용하여 Omi 에 누수 없이 연결하였습니다 (그림 2). 직관적인 Android 앱 (태블릿 실행) 을 통해 여러 대의 Omi 를 동시에 제어할 수 있습니다 (그림 2).
이 앱을 통해 사용자는 흐름 프로파일을 구성하고, 캘리브레이션 및 세척 절차를 수행할 수 있습니다. 원하는 흐름 프로파일 및 시간 범위를 설정한 후 (그림 1), 소량의 배지 (3.3 mL) 를 Omi 에 추가합니다. 마지막으로 실험을 시작하고, Omi 를 인큐베이터로 이동시킵니다 (그림 2).

그림 1 실험 워크플로우 개요

3. 면역형광 염색 및 이미징
시료는 고정 (fixation), 투과화 (permeabilization), 블로킹 (blocking) 처리를 거친 후, 1 차 항체 (VE-cadherin 및 GM130) 와 함께 하룻밤 동안 배양하였습니다. 이후 2 차 항체 및 DAPI 로 염색하였습니다. 이미징은 20 배 대물렌즈가 장착된 EVOS M7000 현미경 (Thermo Fisher Scientific) 을 사용하여 수행하였습니다. 각 채널당 무작위 위치에서 6 장의 이미지를 촬영하였으며, 조건당 4 개의 기술적 반복 (technical replicates) 을 사용하였습니다.
4. hiPSC-EC 정렬 및 극화의 정량화
면역형광 이미지는 PolarityJam⁶ 을 사용하여 분석하였으며, 이를 통해 hiPSC 유래 내피 세포 (hiPSC-ECs) 의 정렬 및 극화를 정량화하였습니다. 모든 이미지는 PolarityJam 에서 분석하였고, 데이터를 통합하여 방향성 및 극화 그래프를 작성하였습니다.
결과: 안정적인 단방향 흐름이 hiPSC 유래 내피 세포의 정렬 및 극화를 유도함
1. 재순환을 통한 안정적인 단방향 흐름 프로파일
hiPSC-ECs 를 지원하고 흐름 방향에 평행한 정렬을 부드럽게 촉진하기 위해, 그림 3A 에 명시된 대로 흐름 프로파일을 설정하였습니다. 유량은 24 시간마다 증가시켰으며, 최대 200 μL/min (전단 응력 0.912 dyn/cm² 에 해당) 으로 48 시간 동안 유지하였습니다. Omi 는 이러한 유량을 지속적으로 유지할 수 있었으며, 지정된 시간 포인트에서 더 높은 유량으로 안정적으로 전환할 수 있었습니다 (그림 3B).
재순환 주기마다 최대 1 분간 흐름이 정지되는 리필 (refill) 단계가 뒤따른다는 점에 유의하시기 바랍니다. 이는 그래프에서 유량이 0 μL/min 으로 하락하는 구간으로 확인할 수 있습니다. 재순환 기능 덕분에 실험 중 추가적인 배지 공급이 필요하지 않았습니다. 단방향 흐름은 VE-cadherin 에 대한 면역염색 후 정성적 관찰에서 확인할 수 있듯이 (그림 3C), hiPSC-ECs 가 흐름 방향에 평행하게 강하게 정렬되도록 유도하였습니다.

그림 3 흐름 제어 및 다양한 조건 하의 내피 세포 반응
(A) 실험에 사용된 유량 (flowrates) 및 시간 간격 (time intervals) 표
(B) Omi 가 다양한 유량 간 전환이 가능하고, 재순환 기능을 제공하면서도 장시간에 걸쳐 해당 유량을 안정적으로 유지할 수 있음을 보여주는 대표 흐름 트레이스 (flow traces)
(C) 정적 조건 (static), 양방향 흐름 조건 (록킹 플랫폼 사용), 단방향 흐름 조건 (Omi 사용) 에서 배양된 hiPSC 유래 내피 세포 (hiPSC-ECs) 의 면역형광 이미지
2. hiPSC-EC 정렬 및 극화의 정량화
PolarityJam⁶ 을 활용하여 hiPSC-EC 의 정렬 및 극화를 정량화할 수 있었습니다 (그림 4A). 5 일 후, Omi 를 이용한 단방향 흐름을 적용한 조건에서 hiPSC-ECs 는 강하게 극화되었으며 흐름 방향에 평행하게 정렬되었습니다 (그림 4A 좌측 이미지 및 그림 4B 상단 그래프).
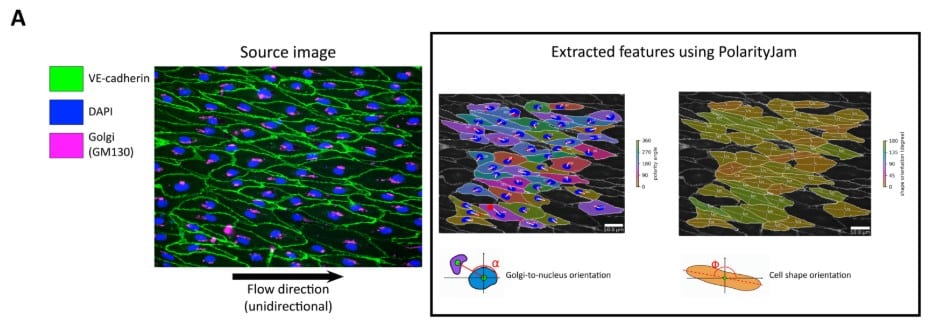

그림 4. 흐름 의존적 내피 세포 정렬 및 극성 평가
(A) 세포 특성 추출 (PolarityJam) 에 사용된 대표 면역형광 이미지. hiPSC-ECs 는 VE-cadherin (녹색) 및 골지체 (GM130, 분홍색) 에 대해 면역염색되었습니다. 핵과 골지체 사이의 각도를 ‘골지체 -핵 방향 (golgi-nucleus orientation)’으로 정의하며, 이는 hiPSC-EC 극화 판정에 사용됩니다. 세포 형태 방향성은 hiPSC-ECs 가 흐름 방향에 평행하게 정렬되었는지를 나타내는 지표로 활용됩니다.
(B) Omi 가 제공하는 지속적 단방향 흐름 및 전단력은 세포 형태 방향성이 흐름 방향과 강하게 평행하게 정렬되도록 유도하였습니다. 또한, 단방향 흐름은 골지체 -핵 방향의 극화를 유도하였으며, 이는 흐름 방향과 정확히 반대되는 극성 지수 (polarity index) 및 음의 V-score 로 입증되었습니다. 이러한 효과는 정적 조건 및 양방향 흐름 조건에서는 관찰되지 않았습니다. N (분석된 세포 수) 은 조건마다 다르며, n (기술적 반복 수) = 4 입니다.
중요하게도, 단방향 흐름은 원형 플롯 및 극성 지수 (0.174, 그림 4B 하단 그래프) 에서 확인할 수 있듯이 골지체 -핵 극화를 유도하였습니다. 골지체 -핵 극화의 평균 방향은 흐름 방향과 반대 (빨간색 화살표) 로 나타나, 흐름이 극화를 유도했음을 시사합니다.
극성 지수는 빨간색 화살표의 길이로 시각화되며, 극화 정도를 나타내는 척도로 값이 클수록 더 강한 극화를 의미합니다. 정적 조건 및 양방향 조건에서는 각각 극성 지수가 0.06 및 0.0243 으로, 이러한 효과가 관찰되지 않았습니다. 또한, 단방향 흐름 시료의 더 높은 음의 V-score (-0.174, 흐름 방향과의 일치도 척도) 는 흐름 방향과 반대되는 극화를 지지하는 결과입니다.
종합하면, 이러한 데이터는 상대적으로 낮은 최대 전단 응력 (0.912 dyn/cm²) 에서도 Omi 가 제공하는 단방향 흐름이 생리학적 관련성을 갖춘 내피 세포 (EC) 표현형을 유도함을 시사합니다. 따라서 더 높은 전단 응력을 사용할 경우, hiPSC-ECs 의 더 강력한 골지체 -핵 극화를 유도할 수 있을 것으로 추론됩니다. 본 연구에서 입증된 안정적인 단방향 흐름은 정확한 혈관 체외 모델링에 필수적이며, hiPSC-ECs 가 성숙하고 생리학적 관련성을 갖춘 표현형을 획득하는 데 기여할 수 있습니다.
결론 및 향후 방향
결과 요약
본 연구는 Omi™ 플랫폼이 운용의 간편성과 생물학적 정교함을 성공적으로 연결함을 확인하였습니다.
실제로, Omi™ 플랫폼은 생리학적 조건을 밀접하게 재현하는 혈관 온 칩 (vessel-on-chip) 모델에서 장기적·저용량 재순환 관류를 수행하도록 설정할 수 있습니다.
운용의 간편성과 생물학적 관련성을 갖춘 흐름 조건을 결합함으로써, Omi™ 플랫폼은 자동화된 재순환 기능을 갖춘 안정적인 단방향 관류를 지원합니다. 이 구성을 통해 연구자들은 다음을 수행할 수 있습니다:
- 혈전증 또는 동맥경화증과 같은 병리적 혈관 조건 재현
- 특화된 혈관 모델 내 면역 세포 외유출 (extravasation) 연구
- 조절된 흐름 하에서 염증 반응에 대한 견고한 연구 수행
5 일간, Omi™ 는 안정적인 자동화 단방향 흐름을 유지하였으며, 이는 성숙한 내피 세포 표현형 달성에 결정적인 요소였습니다.
정적 조건 및 양방향 (록킹) 조건은 세포 조직화를 유도하지 못했으나, Omi™ 기반 환경은 다음을 유도하였습니다:
- 정밀한 형태학적 정렬: hiPSC-ECs 가 흐름 벡터에 평행하게 정렬
- 기능적 극화: 골지체 -핵 방향성의 유의미한 변화, 생리학적 성숙 지표
- 배지 효율성: 연속 재순환을 통해 극히 적은 배지 부피로 결과 달성
OoC 생태계 전반의 다용도성
또한, Omi™ 플랫폼은 범용 통합을 위해 설계되었습니다. 유연한 커넥터 인터페이스를 통해 연구자는 모든 미세유체 칩과 연결할 수 있어, 표준 장기 온 칩 (OoC) 설정을 최소한의 설정 노력으로 고정밀 관류 혈관 모델로 전환할 수 있습니다.
연구 지평 확장
안정적인 장기 관류 환경을 제공함으로써, Omi™ 는 복잡한 혈관 연구를 위한 새로운 가능성을 열어줍니다:
- 병리적 모델링: 동맥경화증 또는 혈전증의 혈역학적 조건 시뮬레이션
- 면역학 연구: 특화된 혈관 온 칩 장벽 내 면역 세포 외유출 및 유도 메커니즘 규명
- 신약 개발: 현실적인 흐름 조건 하에서 고정밀 염증 반응 분석 수행
- 맞춤형 의학: 환자 특이적 hiPSC 를 활용한 혈관 약물 독성 또는 효능 예측
Omi 의 작동 원리에 대해 더 알아보기:
🚀 혈관 연구를 한 단계 업그레이드할 준비가 되셨나요?
데이터는 명확합니다: 단방향 흐름은 생리학적 관련성을 확보하는 핵심 요소입니다. 정적 배양이나 최적화되지 않은 록킹 플랫폼으로 타협하지 마십시오.
Omi™ 의 차별화된 우위를 경험해 보세요
- 데모 요청: Omi™ 플랫폼이 기존 미세유체 칩과 어떻게 연동되는지 확인해 보십시오.
- 전문가 상담: 당사의 응용 과학자와 동맥경화증, 혈전증 또는 면역 세포 외유출 모델링에 대해 논의해 보십시오.
관련 솔루션 및 전문 기술
감사의 글
라이덴 OoC 센터와 오를로바 박사의 연구는 다음 기관 및 프로젝트의 지원을 받았습니다.
림프칩 프로젝트, 연구비 번호: NWA-ORC 2019 1292.19.019, 네덜란드 과학 연구 기구(NWO)의 “컨소시엄 기반 연구(ORC)” 프로그램의 일환으로 지원됨.
노보 노르디스크 재단 줄기세포 의학 센터, 연구비 번호: NNF21CC0073729
References
1. Ingber DE. Human organs-on-chips for disease modelling, drug development and personalized medicine. Nat Rev Genet. 2022 Aug;23(8):467–91.
2. Shakeri A, Wang Y, Zhao Y, Landau S, Perera K, Lee J, et al. Engineering Organ-on-a-Chip Systems for Vascular Diseases. Arterioscler Thromb Vasc Biol. 2023 Dec;43(12):2241–55.
3. Jang S, Collin de l’Hortet A, Soto-Gutierrez A. Induced Pluripotent Stem Cell-Derived Endothelial Cells: Overview, Current Advances, Applications, and Future Directions. Am J Pathol. 2019 Mar;189(3):502–12.
4. Orlova VV, van den Hil FE, Petrus-Reurer S, Drabsch Y, Ten Dijke P, Mummery CL. Generation, expansion and functional analysis of endothelial cells and pericytes derived from human pluripotent stem cells. Nat Protoc. 2014;9(6):1514–31.
5. Tkachenko E, Gutierrez E, Saikin SK, Fogelstrand P, Kim C, Groisman A, et al. The nucleus of endothelial cell as a sensor of blood flow direction. Biol Open. 2013 Aug 14;2(10):1007–12.
6. Dorland YL, Huveneers S. Cell-cell junctional mechanotransduction in endothelial remodeling. Cell Mol Life Sci CMLS. 2017 Jan;74(2):279–92.
7. Giese W, Albrecht JP, Oppenheim O, Akmeriç EB, Kraxner J, Schmidt D, et al. Polarity-JaM: an image analysis toolbox for cell polarity, junction and morphology quantification. Nat Commun. 2025 Feb 8;16(1):1474.



