面临的挑战:为什么单向流至关重要
体外模型有望通过补充、减少甚至潜在替代动物实验,彻底改变生物医学研究的现状。结合人诱导多能干细胞(hiPSCs)及获取器官特异性细胞的分化方案,科学家可以构建先进的人类体外模型,用于开发新药、揭示人类疾病机制以及推动个性化医疗的发展1,2。微流控器官芯片(OoC)模型尤为适合此类研究,因为它们在可灌注的微米级腔室内培养活体人类细胞,以微型化的形式高度模拟组织和器官的功能1–3。
在人体中,健康的动脉和静脉承受着持续的层流剪切应力。为了在体外完美复制这一环境,仅靠静态培养或双向(摇床)流动是远远不够的。
- 静态培养:会导致非生理性的“鹅卵石”状细胞形态。
- 双向流:模拟的是受扰动的病理状态(例如动脉粥样硬化)。
- 单向流:是诱导成熟、静息内皮表型的关键所在。
解决方案:Omi™ OoC平台
Fluigent的Omi是一款紧凑且易于使用的微流控系统。研究人员可以利用它轻松连接自己关注的器官芯片模型,并建立带有液体循环功能的微流控单向流实验。Omi™将复杂的微流控技术大幅简化,转化为一个用户友好的自动化系统。
血管建模的核心功能:
- 持续循环:仅需极少量的培养基(3.3 mL),即可维持长达5天以上的稳定流态。
- 广泛兼容性:通过标准鲁尔接头(Luer fittings)可无缝连接任何芯片(例如Beonchip Be-Flow)。
- 智能控制:直观的安卓操作界面,便于进行精准校准和流量编程。
实验结果:一目了然
在本应用说明中,我们使用连接了Beonchip Be-Flow芯片的Omi系统,进行了为期5天的单向流实验。芯片内提前接种了hiPSC衍生的内皮细胞(hiPSC-ECs)4,5。我们将该条件下的芯片与静态培养的芯片,以及在摇床上进行双向流培养的芯片进行了对比分析。
| 特征 | 静态培养 | 双向流(摇床) | Omi™单向流 |
|---|---|---|---|
| 流动状态 | 无流动 | 间歇/反向流动 | 稳定/持续流动 |
| 细胞形态 | 鹅卵石状 | 随机分布 | 细长且排列整齐 |
| 极化程度 | 无 | 低 (0.024) | 强 (0.174) |
| 剪切应力 | 0 dyn/cm2 | 不固定 | 0.912 dyn/cm2 |
实验流程与定量数据:为期5天的自动化工作流程
本应用说明提供了一套详尽的、循序渐进的实验工作流程,涵盖从细胞接种到定量图像分析的各个环节。
您将了解到:
- 针对hiPSC衍生内皮细胞的5天单向流实验方案
- Omi™的设备设置及循环工作流程
- 静态、双向和单向流动条件的直接对比
- 使用PolarityJam软件对细胞排列和极化进行定量分析
- 在长期培养过程中成功维持稳定流动的实验证据
1 细胞分化、培养与接种
hiPSCs维持在涂有重组玻连蛋白的培养皿中,使用TeSR-E8培养基,每周传代一次。hiPSC-ECs的衍生和日常维持按照Orlova课题组此前描述的方法进行4,5。Beonchip Be-Flow微流控芯片预先涂有50 µg/mL的牛纤连蛋白。将hiPSC-ECs解离并重悬于添加了青霉素-链霉素(PenStrep)的EGM-2培养基中,浓度调整为510^6细胞/mL。小心地将50 µl细胞悬液移液至芯片入口,使细胞被动泵入芯片内部。细胞在37°C下贴壁1小时后,将芯片转移至摇床平台上过夜培养15小时。
第二天,实验正式启动。将芯片分别置于静态培养、继续留在摇床平台上(双向流)或连接至Omi系统(单向流)。
2 Omi系统设置
使用Omi软件创建了一个为期5天的自动化循环实验方案,并将其加载至Omi设备上(图2A)。该软件通过内置的逐步说明引导用户完成每一步操作,包括:
1. 校准:设置储液槽液位传感器,以确保流量测量的准确无误。
2. 灭菌:依次用纯水和70%乙醇冲洗Omi的流体路径及实验管路。注意:使用前,所有接头和管路均已通过高压蒸汽灭菌或浸泡在灭菌液中进行了严格消毒。
3. 预充液:用培养基预先填充流体路径,以彻底排除气泡并确保液体的连续流动。
4. 芯片连接:在开始循环灌注之前,将Omi与微流控芯片(Beonchip Be-Flow)稳妥连接(图2)。
包含hiPSC-ECs的微流控芯片(Beonchip Be-Flow)通过标准鲁尔接头和微流控管路连接至Omi,以确保整个连接处绝对防漏(图2)。用户可以通过平板电脑上一款直观的安卓应用程序同时控制多台Omi设备(图2)。
该应用程序还允许用户自主配置流态,并执行校准和清洁程序。在配置好所需的流态参数和时间范围(图1)后,向Omi中加入少量培养基(仅3.3 mL)。最后,启动实验,并将Omi放入标准培养箱中运行(图2)。

图1 实验工作流程概述

3 免疫荧光与成像
对样本进行固定、透化、封闭处理后,与一抗(VE-钙粘蛋白和GM130)过夜孵育,随后进行二抗和DAPI染色。使用配备20倍物镜的EVOS M7000显微镜(Thermo Fisher Scientific)对样本进行高分辨率成像。在每个微通道中随机选择六个位置进行拍摄。每个实验条件均设置四个技术重复。
4 hiPSC-EC排列与极化的定量分析
使用PolarityJam软件6分析免疫荧光图像,以精准量化hiPSC-ECs的排列和极化情况。所有图像均在PolarityJam中进行处理,并汇总数据以绘制细胞方向和极化图表。
实验结果:稳定的单向流驱动hiPSC衍生内皮细胞的排列与极化
1 带循环功能的稳定单向流态
为了更好地支持hiPSC-ECs的生长并温和地促进其顺应流向进行排列,我们按图3A所示配置了流态。流速每24小时提升一次,并维持在200 μL/min的最大流速(对应剪切应力为0.912 dyn/cm²)长达48小时。Omi能够持续稳定地维持这些流速,并在指定的时间点平稳切换到更高的流速(图3B)。
需要特别指出的是,每个循环周期结束后都会伴随一个重新充液的过程,此时水流会暂停最多一分钟(从图表中流速降至0 μL/min的节点可以看出)。得益于系统的循环特性,实验期间无需额外补充任何培养基。对VE-钙粘蛋白进行免疫染色后的定性观察清晰地表明,单向流促使hiPSC-ECs沿流动方向实现了高度一致的排列(图3C)。

图3 不同条件下的流量控制与内皮细胞生理响应
(A) 实验中使用的流速和时间间隔汇总表。
(B) 具有代表性的流量轨迹图,表明Omi能够在不同流速间精准切换,并在提供循环功能的同时长时间维持设定流速。
(C) 分别在静态、双向流(使用摇床)和单向流(使用Omi)条件下培养的hiPSC-ECs的免疫荧光图像。
2 hiPSC-EC排列与极化的定量分析
借助PolarityJam软件6,我们可以对hiPSC-EC的排列和极化情况进行定量分析(图4A)。在使用Omi施加单向流五天后,hiPSC-ECs表现出极其强烈的极化,并完美平行于流动方向排列(图4A左图及图4B上部图表)。
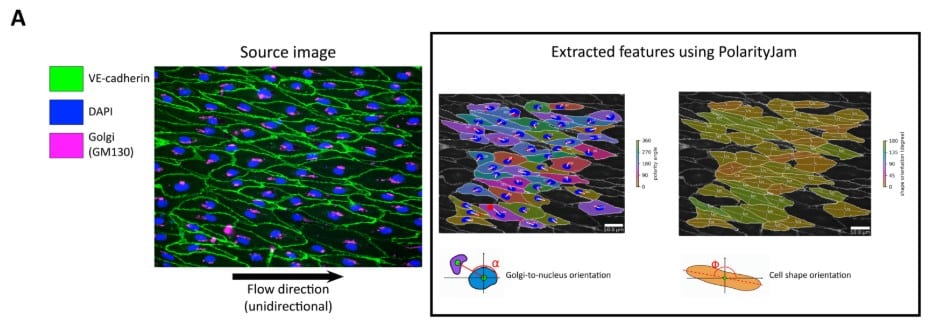

图4. 依赖于流动的内皮细胞排列与极性综合评估
(A) 用于提取细胞特征(PolarityJam)的代表性免疫荧光图像。对hiPSC-ECs进行了VE-钙粘蛋白(绿色)和高尔基复合体(GM130,粉色)的免疫染色荧光标记。细胞核与高尔基体之间的夹角被定义为高尔基体-细胞核方向,用于确定hiPSC-EC的极化程度。细胞形态的朝向则用于指示hiPSC-ECs是否平行于流动方向有序排列。
(B) Omi提供的连续单向流和剪切力使得细胞形态强烈地顺应流向排列。此外,单向流还成功诱导了高尔基体-细胞核方向的极化,这从指向与流向完全相反的极性指数以及负V分数中可以得到有力证实。这些显著效应在静态和双向流条件下均未出现。N(分析的细胞数量)因具体条件而异。n(技术重复次数)= 4。
尤为重要的是,单向流引起了高尔基体-细胞核的显著极化,这从极坐标图和极性指数(0.174,图4B底部图表)中一目了然。高尔基体-细胞核极化的平均方向与流体的流动方向(红色箭头)截然相反,充分表明正是流体剪切力诱导了这种极化现象。
极性指数通过红色箭头的长度进行直观可视化,它是衡量细胞极化程度的关键指标,数值越大代表极化越强。静态和双向流条件均未能表现出此效应,其极性指数仅为极低的0.06和0.0243。此外,单向流样本中较高的负V分数(-0.174,一种衡量与流向一致性的统计算法指标)进一步支撑了这一结果,明确表明极化方向与流向相反。
综上所述,这些确凿的数据表明,由Omi提供的单向流能够成功诱导出具有高度生理相关性的内皮细胞(EC)表型,即使在最高剪切应力相对较低(0.912 dyn/cm²)的情况下依然如此。因此可以合理推测,当应用更高的剪切应力时,能够诱导hiPSC-ECs产生更强的高尔基体-细胞核极化。本文所展示的稳定单向流对于准确进行体外血管建模具有不可替代的作用,并能切实帮助hiPSC-ECs获得成熟且相关的生理表型。
结论与未来展望
实验结果总结
本项研究充分证实,Omi™平台成功地在操作的简便性与生物系统的复杂性之间架起了一座桥梁。
事实上,Omi™平台可以轻松设置,在高度还原真实生理条件的血管芯片模型中执行长期、低体积的循环灌注。
通过将极致简便的操作与具有高度生物相关性的流动条件完美结合,Omi™平台支持带有自动循环功能的稳定单向灌注。这种配置使研究人员能够:
这种配置使研究人员能够:
- 逼真重现血栓形成或动脉粥样硬化等病理性血管状况。
- 在特定的血管模型中深入研究免疫细胞的外渗机制。
- 在受控流动条件下对炎症反应进行高度可靠的研究。
在为期五天的实验周期内,Omi™始终维持着稳定、自动化的单向流,这也是实现成熟内皮细胞表型的决定性因素。
虽然静态和双向(摇床)条件均未能诱导细胞的有序排列,但Omi™驱动的流体环境成功触发了以下结果:
- 培养基的高效利用:连续循环机制让我们能够以极低的培养基消耗量实现上述卓越成果。
- 精确的形态学排列:促使hiPSC-ECs完美平行于流动矢量方向排列。
- 功能性极化:产生了显著的高尔基体-细胞核取向,标志着细胞已达到生理成熟状态。
器官芯片(OoC)生态系统中的多功能性
此外,Omi™平台专为实现通用集成而设计。其灵活的连接接口允许研究人员将其与任何微流控芯片轻松配对,只需极少的准备工作,即可将标准的器官芯片(OoC)装置瞬间转化为高保真的灌注型血管模型。
不断拓展的研究视野
通过提供稳定、长期的灌注环境,Omi™为复杂的血管研究开启了全新的大门,应用领域包括:
- 病理建模:精准模拟动脉粥样硬化或血栓形成时的血流动力学变化。
- 免疫学研究:在特定的血管芯片屏障内,深入探究免疫细胞的外渗和募集过程。
- 药物发现:在逼真的流动条件下进行高保真的炎症反应分析测试。
- 个性化医疗:利用患者特异性的hiPSCs,前瞻性地预测血管类药物的毒性或实际疗效。
进一步阅读以深入了解Omi的工作原理:
🚀您准备好将血管研究提升到新高度了吗?
实验数据已经非常明确:单向流是提高生理相关性的绝对关键。请不要再向静态培养或不够理想的摇床平台妥协了。
即刻体验Omi™的独特优势
- 申请产品演示:亲眼见证Omi™平台如何与您现有的微流控芯片实现无缝整合。
- 咨询专业技术专家:与我们的应用科学家一对一交流,探讨如何构建完美的动脉粥样硬化、血栓形成或免疫细胞外渗模型。
相关解决方案与专业技术
致谢
莱顿器官芯片中心(Leiden OoC Center)及 Orlova 博士的研究工作,由以下机构与项目资助支持:
LymphChip 项目,项目编号:NWA-ORC 2019 1292.19.019,隶属于荷兰科学研究组织(NWO)资助的 NWA 研究计划”联盟研究路径计划”(Research on Routes by Consortia, ORC)。
诺和诺德基金会干细胞医学中心(Novo Nordisk Foundation Center for Stem Cell Medicine),资助项目编号:NNF21CC0073729;
References
1. Ingber DE. Human organs-on-chips for disease modelling, drug development and personalized medicine. Nat Rev Genet. 2022 Aug;23(8):467–91.
2. Shakeri A, Wang Y, Zhao Y, Landau S, Perera K, Lee J, et al. Engineering Organ-on-a-Chip Systems for Vascular Diseases. Arterioscler Thromb Vasc Biol. 2023 Dec;43(12):2241–55.
3. Jang S, Collin de l’Hortet A, Soto-Gutierrez A. Induced Pluripotent Stem Cell-Derived Endothelial Cells: Overview, Current Advances, Applications, and Future Directions. Am J Pathol. 2019 Mar;189(3):502–12.
4. Orlova VV, van den Hil FE, Petrus-Reurer S, Drabsch Y, Ten Dijke P, Mummery CL. Generation, expansion and functional analysis of endothelial cells and pericytes derived from human pluripotent stem cells. Nat Protoc. 2014;9(6):1514–31.
5. Tkachenko E, Gutierrez E, Saikin SK, Fogelstrand P, Kim C, Groisman A, et al. The nucleus of endothelial cell as a sensor of blood flow direction. Biol Open. 2013 Aug 14;2(10):1007–12.
6. Dorland YL, Huveneers S. Cell-cell junctional mechanotransduction in endothelial remodeling. Cell Mol Life Sci CMLS. 2017 Jan;74(2):279–92.
7. Giese W, Albrecht JP, Oppenheim O, Akmeriç EB, Kraxner J, Schmidt D, et al. Polarity-JaM: an image analysis toolbox for cell polarity, junction and morphology quantification. Nat Commun. 2025 Feb 8;16(1):1474.






